إحياء بطاريات أيونات الصوديوم في درجة حرارة الغرفة
نظرًا لاحتياطيات الصوديوم الوفيرة (Na) في القشرة الأرضية والخصائص الفيزيائية والكيميائية المماثلة للصوديوم والليثيوم، فإن تخزين الطاقة الكهروكيميائية القائمة على الصوديوم يحمل وعدًا كبيرًا لتخزين الطاقة على نطاق واسع وتطوير الشبكات. على سبيل المثال، أثبتت خلايا النشاط البحثي للبطاريات ذات الانبعاثات الصفرية ذات درجة الحرارة العالية المستندة إلى أنظمة Na/NiCl وخلايا Na-S ذات درجة الحرارة العالية، والتي تعد حالات تجارية ناجحة للتطبيقات الثابتة والمتنقلة، إمكانات البطاريات القابلة لإعادة الشحن المعتمدة على الصوديوم. ومع ذلك، فإن درجة حرارة التشغيل المرتفعة التي تبلغ حوالي 300 درجة مئوية تسبب مشكلات أمنية وتقلل من كفاءة بطاريات أيون الصوديوم (SIBs) ذهابًا وإيابًا. لذلك تعتبر SIBs في درجة حرارة الغرفة (RT) على نطاق واسع هي التكنولوجيا البديلة الواعدة لـ LIBs.
على مدار تاريخ البطاريات في المائتي عام الماضية، تم إجراء الأبحاث على SIBs بحماس جنبًا إلى جنب مع تطوير LIB. تم طرح النشاط الكهروكيميائي لـ TiS2 للليثيوم وجدواه لتخزين الطاقة لأول مرة في السبعينيات. بعد هذا الاكتشاف، تم تحقيق إمكانية إدراج أيونات الصوديوم في TiS+2 في أوائل الثمانينيات. مع اكتشاف الجرافيت باعتباره مادة أنود منخفضة التكلفة ومتوسطة السعة للـ LIBs والفشل في إقحام أيونات الصوديوم، حدث تطور سريع للـ LIB في التسعينيات، ليحل محل النمو في كيمياء الصوديوم. ثم، في عام 2000، أدى توفر تخزين الصوديوم في الكربون الصلب (HC)، والذي من شأنه أن يوفر قدرة طاقة مماثلة لتلك الموجودة في الليثيوم في الجرافيت، إلى تجديد الاهتمام البحثي في SIBs.
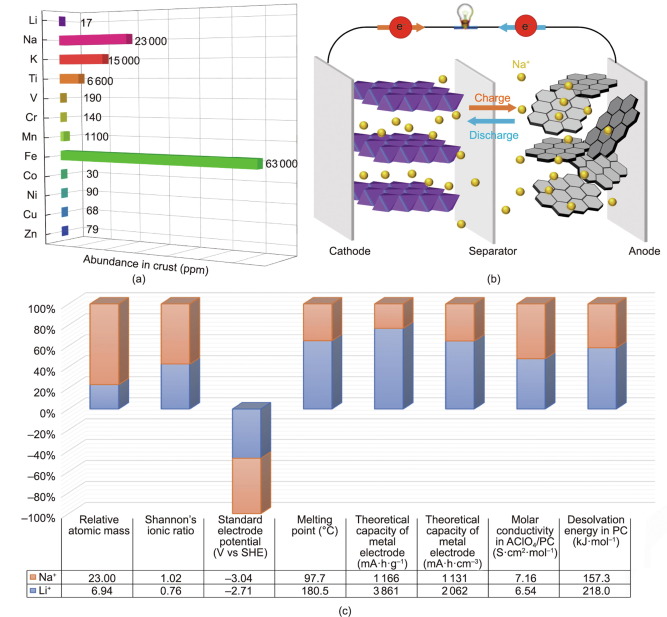
مقارنة بين بطارية أيون الصوديوم وبطارية أيون الليثيوم
إن إحياء الـ SIBs - إلى جانب الضغط المتزايد باستمرار بسبب عدم توفر احتياطيات الليثيوم والتصاعد المقابل في التكلفة - يوفر استراتيجية تكميلية للـ LIBs. اكتسبت عقود الأثر الاجتماعي اهتمامًا بحثيًا متزايدًا، جنبًا إلى جنب مع الإنجازات الأساسية في علوم المواد، في محاولة لتلبية الاختراق المتزايد لتقنيات الطاقة المتجددة. تتطابق مكونات الخلية وآليات التفاعل الكهروكيميائي في SIBs بشكل أساسي مع تلك الموجودة في LIBs، باستثناء حامل الشحنة، وهو Na في أحدهما وLi في الآخر. يُعزى السبب الرئيسي للتوسع السريع في كيمياء مواد SIB إلى أوجه التشابه في الخواص الفيزيائية والكيميائية بين المعدنين القلويين.
أولاً، تتشابه مبادئ التشغيل وبناء الخلايا لـ SIBs مع مبادئ LIBs التجارية، على الرغم من أن Na يعمل كحامل الشحنة. توجد أربعة مكونات رئيسية في SIB النموذجي: مادة الكاثود (عادةً مركب يحتوي على Na)؛ مادة الأنود (لا تحتوي بالضرورة على الصوديوم)؛ المنحل بالكهرباء (في حالة سائلة أو صلبة)؛ وفاصل. أثناء عملية الشحن، يتم استخراج أيونات الصوديوم من الكاثودات، والتي عادة ما تكون عبارة عن طبقات من أكاسيد المعادن ومركبات بولي أنيونية، ثم يتم إدخالها في الأنودات، بينما ينتقل التيار عبر دائرة خارجية في الاتجاه المعاكس. عند التفريغ، يترك Na الأنودات ويعود إلى الكاثودات في عملية يشار إليها باسم "مبدأ الكرسي الهزاز". وقد مكنت أوجه التشابه هذه من الفهم الأولي لتكنولوجيا SIB والنمو السريع فيها.
علاوة على ذلك، فإن نصف القطر الأيوني الأكبر لـ Na يجلب مزاياه الخاصة: زيادة مرونة الإيجابية الكهروكيميائية وانخفاض طاقة إزالة الذوبان في المذيبات القطبية. عادةً ما تؤدي الفجوة الأكبر في نصف القطر الأيوني بين Li وأيونات المعادن الانتقالية إلى فشل مرونة تصميم المواد. في المقابل، يتيح النظام المعتمد على الصوديوم هياكل صلبة أكثر مرونة من النظام المعتمد على الليثيوم، ويمتلك موصلية أيونية هائلة. والمثال النموذجي هو β-Al2O3، حيث يتمتع إقحام Na بالحجم المثالي والموصلية العالية. يمكن بسهولة تحقيق المزيد من أكاسيد الفلزات الانتقالية ذات الطبقات بطرق تكديس M+x+ مختلفة في نظام قائم على الصوديوم. وبالمثل، فإن المجموعة الواسعة من الهياكل البلورية المعروفة بعائلة الموصلات الأيونية للصوديوم (NaSICON) أكثر تعقيدًا بكثير من نظائر الليثيوم. والأهم من ذلك، أنه يمكن السماح بموصلية أيونية أعلى بكثير في مركبات NaSICON، والتي تتجاوز بكثير الموصلية الأيونية في مركبات موصل أيون الليثيوم (LiSICON).
أخيرًا وليس آخرًا، أثبتت التحقيقات المنهجية باستخدام مذيبات قطبية لابروتيكية مختلفة أن نصف القطر الأيوني الأكبر لـ Na يسبب طاقة خراب أضعف. يتمتع Li الأصغر بكثافة شحنة سطحية أعلى حول النواة مقارنة بـ Na عندما يمتلك كلاهما نفس التكافؤ. لذلك يتم تثبيت Li ديناميكيًا حراريًا من خلال مشاركة المزيد من الإلكترونات مع جزيئات المذيبات القطبية. وهذا يعني أنه يمكن تصنيف Li كنوع من حمض لويس. ونتيجة لذلك، هناك حاجة إلى طاقة خراب عالية نسبيًا للـ Li عالي الاستقطاب، مما يؤدي إلى مقاومة نقل كبيرة نسبيًا ناجمة عن نقل Li من الحالة السائلة (المنحل بالكهرباء) إلى الحالة الصلبة (القطب). نظرًا لأن طاقة الخراب ترتبط ارتباطًا وثيقًا بحركية النقل التي تحدث عند الواجهة السائلة/الصلبة، فإن طاقة الخراب المنخفضة نسبيًا تعد ميزة كبيرة لتصميم SIBs عالية الطاقة.